Химическая сущность процесса мыловарения
Несмотря на то что в конце эпохи средневековья в разных странах существовала довольно развитая мыловаренная промышленность, химическая сущность процессов, конечно, была не ясна. Лишь на рубеже XVIII и XIX вв. была выяснена химическая природа жиров и внесена ясность в реакцию их омыления. В 1779 г. шведский химик Шееле показал, что при взаимодействии оливкового масла с оксидом свинца и водой образуется сладкое и растворимое в воде вещество. Решающий шаг на пути изучения химической природы жиров был сделан французским химиком Шеврелем.
Он открыл стеариновую, пальмитиновую и олеиновую кислоты, как продукты разложения жиров при их омылении водой и щелочами. Сладкое вещество, полученное Шееле, было Шеврелем названо глицерином. Сорок лет спустя Бертло установил природу глицерина и объяснил химическое строение жиров. Глицерин – трехатомный спирт. Жиры – сложные эфиры глицерина (глицериды) тяжелых одноосновных карбоновых кислот, преимущественно пальмитиновой CH3(CH2)14COOH, стеариновой CH3(CH2)16COOH и олеиновой CH3(CH2)7CH = CH(CH2)7COOH. Их формулу и реакцию гидролиза можно описать следующим образом:
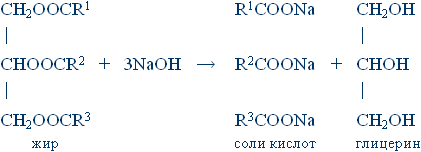
В состав различных жиров входят в различных соотношениях пальмитиновая, стеариновая, олеиновая и другие кислоты. В растительных (жидких) жирах преобладают непредельные кислоты (содержащие этиленовые связи), а в животных (твердых) – предельные кислоты, т.е. не содержащие двойных связей. Потребности в твердых животных жирах большие, чем в растительных. Поэтому жидкие растительные жиры переводят в твердые каталитической гидрогенизацией. В этом процессе остатки непредельных кислот в глицеридах превращаются (присоединением водорода) в остатки предельных кислот. Например:
CH3(CH2)7CH - CH(CH2)7COOH
|
[катализатор 190...240°C]
↓
CH3(CH2)7CH2 - CH2(CH2)7COOH
Именно так получают кулинарные жиры, масло для обжаривания, салатное масло, а также жиры, идущие на производство маргарина. Гидрированные жиры называют саломаслами (сало из масла).
Важно то, что среди остатков различных кислот в глицеридах (жирах) присутствует остаток линолевой кислоты CH3(CH2)4CH = CHCH2CH2CH = CH(CH2)7COOH. В отличие от других эта кислота не синтезируется в организме человека, а вводится только с пищей. В настоящее время существует утвердившееся мнение, что линолевая кислота необходима для предотвращения атеросклероза – распространенной болезни, служащей одной из главных причин потери трудоспособности и преждевременной смерти. Необходимо отметить, что линолевая кислота непредельная, а значит, она входит в состав главным образом растительных жиров.
В быту, не говоря о промышленности, мойке подвергают разные предметы и объекты. Загрязняющие вещества бывают самые разнообразные, но чаще всего они малорастворимы или нерастворимы в воде. Такие вещества, как правило, являются гидрофобными, поскольку водой не смачиваются и с водой не взаимодействуют. Поэтому нужны и различные моющие средства.
Если попытаться дать определение, то мытьем можно назвать очистку загрязненной поверхности жидкостью, содержащей моющее вещество или систему моющих веществ. В качестве жидкости в быту используют главным образом воду. Хорошая моющая система должна выполнять двойную функцию: удалять загрязнение с очищаемой поверхности и переводить его в водный раствор. Значит, моющее средство также должно обладать двойной функцией: способностью взаимодействовать с загрязняющим веществом и переводить его в воду или водный раствор. Следовательно, молекула моющего вещества должна иметь гидрофобную и гидрофильную части. Фобос – по-гречески означает страх, боязнь. Значит, гидрофобность означает боящийся, избегающий воду. Филео – по-гречески – люблю, а гидрофильность – любящий, удерживающий воду. Гидрофобная часть молекулы моющего вещества обладает способностью взаимодействовать с поверхностью гидрофобного загрязняющего вещества. Гидрофильная часть моющего вещества взаимодействует с водой, проникает в воду и увлекает с собой частицу загрязняющего вещества, присоединенную к гидрофобному концу.
Таким образом, моющие вещества должны обладать способностью адсорбироваться на пограничной поверхности, т.е. обладать поверхностной активностью. Их называют поверхностно-активными веществами (ПАВ).
Соли тяжелых карбоновых кислот, например CH3(CH2)14COONa, являются типичными поверхностно-активными веществами. Они содержат гидрофильную часть (в данном случае – карбоксильную группу) и гидрофобную часть (углеводородный радикал).
Животные жиры – древнее и весьма ценное сырье мыловаренной промышленности. Они содержат до 40% (насыщенных) жирных кислот. Искусственные, т.е. синтетические, жирные кислоты получают из парафина нефти каталитическим окислением кислородом воздуха. В упрощенном виде реакцию можно описать следующим уравнением:
CH3(CH2)mCH2 – CH2(CH2)nCH3 + 2,5 O2
↓
CH3(CH2) + CH3(CH2)nCOOH + H2О
Молекула парафина при окислении разрывается в разных местах и потому получается смесь кислот, которые разделяются на фракции. При производстве мыла используют две фракции: C10–C16 и C17–C20. В хозяйственное мыло синтетические кислоты вводят в количестве 35-40%. Для производства мыла также применяют нафтеновые кислоты, выделяемые при очистке нефтепродуктов (бензина, керосина и др.). С этой целью нефтепродукты обрабатывают раствором гидроксида натрия и получают водный раствор натриевых солей нафтеновых кислот (монокарбоновые кислоты ряда циклопентана и циклогексана). Этот раствор упаривают и обрабатывают поваренной солью, в результате чего на поверхность раствора всплывает мазеобразная масса темного цвета – мылонафт. Для очистки мылонафт обрабатывают серной кислотой, т.е. вытесняют из солей сами нафтеновые кислоты. Этот нерастворимый в воде продукт называют асидолом или асидол-мылонафтом. Непосредственно из асидола можно изготавливать только жидкое или, в крайнем случае, мягкое мыло. Оно имеет нефтяной запах, но зато обладает бактерицидными свойствами.
В производстве мыла давно используют канифоль, которую получают при переработке живицы хвойных деревьев. Канифоль состоит из смеси смоляных кислот, содержащих в цепи около 20 углеродных атомов. В рецептуру хозяйственного мыла обычно вводят 12-15% канифоли от массы жирных кислот, а в рецептуру туалетных мыл – не более 10%. Введение канифоли в больших количествах делает мыло мягким и липким.
Процесс производства мыла состоит из химической и механической стадий. На первой стадии (варка мыла) получают водный раствор солей натрия (реже калия) жирных кислот или их заменителей (нафтеновых, смоляных). На второй стадии проводят механическую обработку этих солей – охлаждение, сушку, смешивание с различными добавками, отделку и упаковку.
Варку мыла заканчивают обработкой мыльного раствора (мыльного клея) избытком щелочи (NaOH) или раствором NaCl. В результате этого на поверхность раствора всплывает концентрированный слой мыла, называемый ядром. Полученное таким образом мыло называют ядровым, а процесс его выделения из раствора – отсолкой или высаливанием. При высаливании происходит повышение концентрации мыла и его очистка от белковых, красящих и механических примесей – так получают хозяйственное мыло.
Если мыло варилось из животных или растительных жиров, то из раствора после отделения ядра выделяют образующийся в результате омыления глицерин. Он находит широкое и разнообразное применение: в производстве взрывчатых веществ (тринитроглицерина) и полимерных смол; в качестве умягчителя тканей и кожи; для парфюмерных, косметических и медицинских препаратов; при производстве кондитерских изделий и ликеров. Последним он придает вязкую консистенцию.
Для получения особо чистого и светлого мыла его очищают (шлифуют) переведением снова в раствор кипячением с горячей водой и повторным высаливанием. В результате шлифования мыло приобретает большую однородность, низкую вязкость и надлежащую пластичность. Для изготовления туалетного мыла в очищенном ядровом мыле снижают содержание воды от 30 до 12%. Затем в него вводят парфюмерные отдушки, отбеливатели типа TiO2, красители и др. Хорошие сорта туалетного мыла содержат до 50% мыла, полученного из импортного кокосового или пальмового масла. Кокосовое масло хорошо растворяется в холодной воде и характеризуется высоким пенообразованием. Иногда туалетное мыло содержит до 10% свободных жирных кислот. Самое дорогое туалетное мыло целиком изготавливают из кокосового масла.
Для улучшения некоторых характеристик хозяйственного мыла (иногда и туалетного), а также для удешевления в него вводят наполнители. К ним относятся некоторые натриевые соли (Na2CO3, Na2B4O7, Na5P3O10, жидкое стекло), которые при растворении в воде приводят к подщелачиванию, клеи (казеин, казеиновый студень), углеводы (крахмал). Клеи и крахмал способствуют пенообразованию мыльного раствора и стойкости пены, однако моющей способностью не обладают. Для получения паст в жидкое хозяйственное мыло вводят тонкоизмельченный песок, толченый кирпич, жирные глины. Они способствуют механической очистке. Такие мыла применяют для чистки кухонной посуды, некрашеной мебели, полов и т.д.
Особое место среди наполнителей занимает сапонин, получаемый выщелачиванием некоторых растений и прежде всего мыльного корня. Он хорошо растворяется в воде и его растворы сильно пенятся. Поэтому сапонин используют для улучшения пенообразования и применяют для дорогих сортов мыл. Следует отметить, что замена натрия на калий приводит к изменению консистенции мыла. Из твердого оно становится мягким или мазеобразным. Ионы кальция и магния образуют с анионами тяжелых карбоновых кислот малорастворимые соли. Этот процесс можно выразить уравнениями:
2RCOONa + Ca(HCO3)2 = Ca(RCOO)2 + 2NaHCO3
2RCOONa + MgCl2 = Mg(RCOO)2 + 2NaCl
Поэтому при стирке белья в жесткой воде, содержащей эти ионы, расход мыла повышается на 25-30%. Малорастворимые соли кальция и магния оседают на ткани, забивают поры и потому делают ткань грубой, менее эластичной, с плохой воздухо- и влагопроницаемостью. Такие ткани приобретают сероватый оттенок, а окраска становится блеклой. Кроме того, осевшие на ткани известковые мыла приводят к снижению ее прочности. Это происходит потому, что анионы ненасыщенных карбоновых кислот при сушке тканей окисляются кислородом воздуха с образованием веществ пероксидного характера. Они же окисляют целлюлозу, из которой состоят ткани. Для устранения вредных последствий жесткой воды в мыла вводят натрийтрифосфат Na5P3O10. Анион P3O510– связывает ионы Ca2+ и Mg2+ в прочные, но растворимые в воде соединения. По существу они играют роль умягчителя воды. С этой же целью натрийтрифосфат и другие полифосфатные анионы добавляют и в стиральные порошки.
Кроме использования мыла в качестве моющего средства оно широко применяется при отделке тканей, в производстве косметических средств, для изготовления полировочных составов и водоэмульсионных красок. Имеется и не столь безобидное его применение. Алюминиевое мыло (алюминиевые соли смеси жирных и нафтеновых кислот) применяют в США для получения некоторых видов напалма – самовоспламеняющегося состава, используемого в огнеметах и зажигательных авиабомбах. Само слово напалм происходит от начальных слогов нафтеновой и пальмитиновой кислот. Состав напалма довольно простой – это бензин, загущенный алюминиевым мылом.
В настоящее время химическая промышленность выпускает большое количество различных синтетических моющих средств (стиральных порошков). Наибольшее практическое значение имеют соединения, содержащие насыщенную углеводородную цепь из 10-15 атомов углерода, так или иначе связанную с сульфатной или сульфонатной группой, например
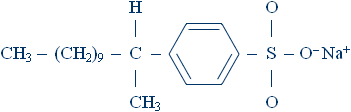
Производство синтетических моющих средств основано на дешевой сырьевой базе, а точнее на продуктах переработки нефти и газа. Они, как правило, не образуют малорастворимых в воде солей кальция и магния.
Следовательно, многие из синтетических моющих средств одинаково хорошо моют как в мягкой, так и в жесткой воде. Некоторые средства пригодны даже для стирки в морской воде. Синтетические моющие средства действуют не только в горячей воде, как это характерно для хозяйственного мыла, но и в воде при сравнительно низких температурах, что важно при стирке тканей из искусственных волокон. Наконец, концентрация синтетических моющих веществ даже в мягкой воде может быть гораздо ниже, чем мыла, полученного из жиров. Синтетические моющие средства обычно представляют довольно сложную композицию, поскольку в них входят различные добавки: оптические отбеливатели, химические отбеливатели, ферменты, пенообразователи, смягчители.
После нескольких стирок изделия из белых тканей желтеют или сереют. Для устранения появляющихся оттенков и вводят в синтетические моющие средства оптические отбеливатели. Их действие заключается в том, что они поглощают ультрафиолетовый свет (с длиной волны ~360 нм) и вновь испускают поглощенную энергию путем флуоресценции в синей области видимого спектра (при 430-440 нм). Возникающее при этом «посинение» изделия компенсирует пожелтение и делает изделие визуально более белым. Действие оптических отбеливателей напоминает действие синьки, с давних пор использовавшейся при полоскании белья после стирки. Бытовая синька или ультрамарин – природный минерал лазурит, называемый также ляпис-лазурью. В монолитном виде он используется как поделочный камень, а его очень тонкий порошок в далеком прошлом применялся в качестве синьки. В 1828 г. ультрамарин был получен искусственно в лабораторных условиях. Для этого смесь каолина, соды и серы прокаливалась в сильной струе воздуха. Состав ультрамарина выражают формулой Na6Al4Si6S4O24, однако его строение до сих пор не выяснено. Заменителем ультрамарина в быту является порошок белой глины (каолина) или мела с предварительно нанесенным на их поверхность органическими красителями синего цвета (органические синьки).
При стирке тканей необходимо не только удалить загрязнения, но и разрушить окрашенные соединения. Часто ими являются природные красители от ягод или вин. Эту функцию выполняют химические отбеливатели. Наиболее распространенным отбеливателем является перборат натрия. Его химическую формулу условно записывают в виде NaBO2·H2O2·3H2О. Из формулы видно, что отбеливающим началом служит пероксид водорода, который образуется в результате гидролиза пербората. Этот химический отбеливатель эффективно действует при 70°C и выше.
Пятна белковых веществ и крови трудно отстирываются и плохо обесцвечиваются химическими отбеливателями. Для их устранения применяют специальные ферменты, которые вводят в качестве добавки к моющим системам. Ферменты действуют при замачивании изделий в холодной воде перед стиркой горячей водой. Однако они могут быть эффективны и непосредственно в процессе стирки.
- Добавить комментарий
- 26350 просмотров




